在人口老龄化加速与全民健康意识提升的双重驱动下,康复器械行业正迎来前所未有的发展机遇。然而,伴随市场扩容而来的是对产品安全性与有效性的更高要求。如何精准判断一款康复器械是否合规?这不仅关乎企业生存发展,更直接关系到使用者的生命健康。本文将深入解读康复器械行业的核心标准体系,结合最新政策动向与行业实践,系统梳理产品合规性的判断维度与实操要点。
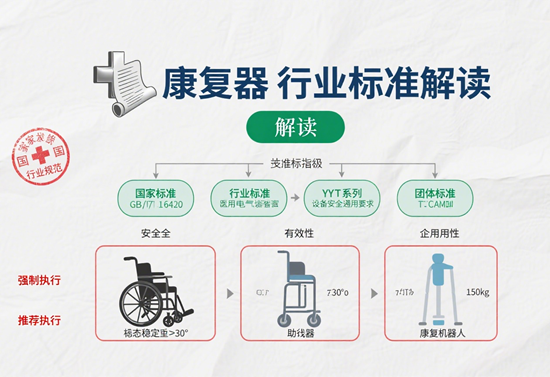
康复器械的合规性判断,首先需立足于国家构建的严密法规标准体系。2021年6月1日起施行的《医疗器械监督管理条例》(国务院令第739号)是行业根本大法,明确了医疗器械全生命周期的监管要求,涵盖研制、生产、经营、使用各环节。紧随其后,《医疗器械临床使用管理办法》(国家卫健委令第8号)于2021年3月1日实施,对医疗机构在临床应用康复器械时的安全管理、规范使用提出了具体指引。这两部法规构成了产品合规的“双支柱”。在国家标准层面,GB/T 41697-2022《康复辅助器具 一般要求和试验方法》为产品性能、安全性、可靠性提供了统一的测试基准。而《养老机构康复辅助器具基本配置》国家标准的发布与实施(如2023年10月1日),则进一步细化了特定场景下康复器械的配置要求与合规边界。企业必须确保产品同时满足上位法规与具体标准的技术规范。
判断产品合规性的核心维度,可从资质审查、技术验证与法规符合性三方面系统把控。资质审查是源头把控的关键。企业需严格核查产品是否取得有效的医疗器械注册证或备案凭证,确认其分类(如一类、二类或三类)与实际风险等级匹配。生产企业的《医疗器械生产许可证》或备案凭证、经营企业的《医疗器械经营许可证》或备案凭证,以及质量管理体系认证(如ISO 13485)等资质文件,均需在有效期内且覆盖对应产品范围。技术验证是合规性的实体支撑。这要求产品性能指标必须符合注册/备案的技术要求,并通过型式检验报告予以证明。安全性验证尤为关键,包括电气安全(如GB 9706系列)、生物相容性(如GB/T 16886)、电磁兼容(如YY 0505)等强制标准检测。产品说明书、标签内容需与注册批准文件完全一致,不得夸大疗效或隐瞒风险。法规符合性则贯穿全流程。生产过程需符合《医疗器械生产质量管理规范》,确保可追溯性;经营与使用环节需遵守《医疗器械临床使用管理办法》,如建立设备验收、维护、不良事件监测制度。广告宣传必须严守《广告法》及医疗广告专项规定,避免出现“根治”“无效退款”等绝对化用语。
时下行业热点正深刻影响合规要求的内涵与外延。2025年全国两会期间,“高端突破”“新技术应用”“设备更新”成为医疗器械领域的核心议题。这预示着融合人工智能、机器人技术的智能康复设备(如外骨骼机器人、脑机接口康复系统)将加速涌现,其合规性面临新挑战:除传统安全标准外,还需关注算法透明度、数据隐私保护(如符合《个人信息保护法》)及人机交互安全性。市场监管总局近期发布的《经颅磁刺激治疗设备校准规范》等医疗健康领域计量技术规范,凸显了对创新型康复器械精准度与稳定性的更高要求。同时,中医药康复服务能力提升工程(2021-2025年)的推进,促使中医类康复器械(如电针仪、艾灸设备)的合规性需同时满足医疗器械法规与中医药特色标准。地方产业政策(如柳州市3亿元投资的康复辅助器械生产项目)的落地,也要求企业在享受政策红利时,同步强化合规建设,避免因标准理解偏差导致项目风险。
康复器械的合规性绝非静态达标,而是动态适应法规演进与技术变革的持续过程。企业需建立“法规雷达”机制,实时跟踪标准更新(如GB/T 41697-2022的修订动态)与监管政策调整(如集采规则对产品成本与质量的新要求)。在产品设计阶段即植入合规基因,通过风险管理(如ISO 14971应用)将标准要求转化为技术参数。最终,唯有将合规视为企业生命线,在创新与规范间找到平衡点,方能在万亿级康复蓝海中行稳致远,真正守护万千使用者的康复之路。